N’hem parlat a l’EMPodCat https://empod.cat/2026/01/29/episodi-52-r-sobre-t/, també en versió vídeo https://www.youtube.com/watch?v=PylaEt07v-E
Camines pel passadís del teu servei d’urgències i veus als teus companys fent compressions toràciques a la persona amb qui has tingut una conversa distesa fa uns minuts, mentre esperàveu els resultats del control de troponines.
Poses els pegats del desfibril·lador, confirmes una fibril·lació ventricular, carregues l’aparell, tothom s’aparta i dispares. Dos minuts més de RCP, segueix en FV i tornes a desfibril·lar.

Aquest cop sí, un cop passats els dos minuts hi ha ritme organitzat al monitor i comproveu que té pols. Ara toca cures postressuscitació i trasllat a destí definitiu.
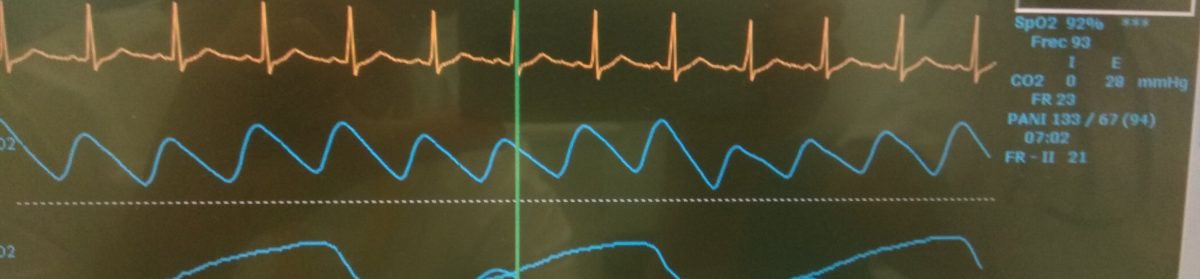
Ara, un cop acabada la feina toca esbrinar que ha passat. Revises el registre del monitor i veus el següent:

En aquesta captura del monitor d’aquesta persona podem veure com es produeix una extrasístole i després el ritme sinusal previ degenera al que sembla una taquicàrdia ventricular polimòrfica i de seguida cap a una fibril·lació ventricular. La corba de pulsioximetria també desapareix de forma sobtada.

Si ens fixem més en detall en el moment de l’extrasístole veiem que aquesta cau una mica abans del pic de l’onda T.
Aquest fenomen, que es coneix com a “R sobre T“, ja es va descriure a la primera meitat del segle passat, quan no feia massa anys que s’havia creat l’electrocardiografia. Consisteix en la superposició d’una extrasístole ventricular (onda R) just sobre l’onda T del batec precedent, per això aquest nom tan descriptiu.
L’extrasistòlia no és pas un fenomen estrany, més o menys tothom té alguna extrasístole de tant. El que fa rellevant aquest R sobre T és el fet que, si es donen les circumstàncies adequades, pot provocar una arrítmia potencialment letal. Aquesta arrítmia acostuma a ser una taquicàrdia ventricular polimòrfica que pot autolimitar-se o degenerar cap a una fibril·lació ventricular.
Perquè aquesta arrítmia tan perillosa es produeixi ha de coincidir que:
- Evidentment, que hi hagi una extrasístole. Com més n’hi hagi més possibilitats que es produeixi el fenomen. Determinades condicions les fan més habituals, una de força perillosa és la isquèmia miocardíaca.
- L’extrasístole es produeixi en el moment en què una part de les cèl·lules miocardíaques ja s’han repolaritzat mentre que una altra part encara està en període refractari. Això fa que una part d’aquestes cèl·lules (les ja repolaritzades) es despolaritzin seguint l’impuls de l’extrasístole mentre altres acaben de repolaritzar-se un cop ja ha passat aquest front de despolarització.
- En la zona propera on s’ha originat l’extrasístole hi hagi un substrat adequat perquè es produeixi una reentrada del front de despolarització. Aquest substrat pot ser una alteració anatòmica, com una cicatriu, o pot ser simplement elèctrica, pel període refractari en aquella zona.
Quan es produeixen aquestes condicions es pot crear un circuit de reentrada. Aquest circuit genera una despolarització “circular” en què els miòcits inicials despolaritzen els seus veïns, cosa que farà despolaritzar els veïns d’aquests i així successivament fins a despolaritzar de nou les cèl·lules que han iniciat la despolarització. És el mateix mecanisme que observem en algunes taquicàrdies supraventriculars. Cal dir que aquest circuit de reentrada, que podem observar al monitoratge electrocardiogràfic com a taquicàrdia ventricular o torçada de puntes, pot degenerar de forma molt ràpida en fibril·lació ventricular, com és el cas d’aquesta entrada.

I què hem de fer un cop ens trobem en aquesta situació? Doncs és bastant “senzill”, tractar el pacient, i si està en aturada cardíaca seguir l’algoritme de ritme desfibril·lable.
El que potser és més important és prevenir aquesta situació de R sobre T abans no es produeixi. Aquestes són algunes de les coses que podem fer:
- Monitoratge electrocardiogràfic supervisat en els pacients de risc: tot pacient en un servei d’urgències amb sospita d’arrítmies, pèrdues de coneixement no explicades o sospita d’oclusió coronària s’hauria de monitorar, almenys les derivacions bipolars. Aquest monitoratge cal que sigui supervisat, si el monitor mostra l’arrítmia, però ningú la veu, de poc ens servirà.
- Posar preventivament els pegats de desfibril·lació en els pacients en risc: És una mesura de prevenció secundària, no ens evitarà que el pacient faci l’arrítmia, però ens permetrà tractar-la de forma immediata.
- Disminuir la possibilitat de fer extrasístoles: Aquesta actuació tan evident no és tan senzilla com sembla. Les causes de les extrasístoles són moltes i excedeixen el que vull parlar en aquesta entrada. Alguns tractaments que es poden fer, segons l’etiologia, van des d’ablacions programades fins a l’administració de fàrmacs. En el cas dels fàrmacs tenim des de l’ús de blocadors beta, antiarrítmics o fins i tot fàrmacs per accelerar la freqüència en el cas que l’extrasistòlia es relacioni amb la bradicàrdia.
- Reduir el temps de risc: com més temps hi ha entre la despolarització (QRS) i la repolarització (T) més possibilitats tenim que l’extrasístole caigui sobre la part ascendent de l’ona T. Aquí és molt important tractar l’allargament de QT, ja que és un factor que predisposa l’R sobre T. De nou, aquí el tractament és segons etiologia. Potser insistir a evitar l’ús concomitant de fàrmacs que poden allargar aquest QT i corregir precoçment els desajustos electrolítics que es relacionen amb aquest allargament com poden ser la hipopotassèmia o la hipomagnesèmia.
- Resoldre l’aparició de substrat adequat: d’aquesta estratègia poca cosa podrem fer a urgències. En ambulatori es poden plantejar cirurgia o ablacions. En el cas d’isquèmia coronària el tractament que haurem d’aplicar per resoldre-la ja ens disminuirà aquest risc, tot i que el moment de la reperfusió ens pot generar alguna arrítmia. En cas que aquest substrat no es pugui resoldre, la implantació d’un desfibril·lador implantable pot ser una teràpia salvadora per les persones en risc.
Aquí és on acabaria aquesta entrada, però com us quedeu si us dic que aquest fenomen també es pot provocar de forma externa?
De fa segles, almenys des del XVIII, s’han descrit casos de mort per contusions al centre del tòrax, de vegades, aparentment banals. A aquesta condició se la coneix com a commotio cordis. En els últims decennis s’ha estudiat amb més profunditat a causa de la seva incidència en l’esport.
Aquí, la “R” no és una extrasístole, sinó un impacte extern, habitualment al centre del tòrax, amb l’energia molt concentrada en un punt, com podria ser un impacte d’una pilota petita o un disc. Aquest impacte mecànic pot produir una despolarització igual que l’extrasistòlia, potser els més antics recordareu el cop de puny precordial o el marcapassos de puny. Igual que passa en l’R sobre T, si aquesta despolarització es produeix en el moment adequat es pot entrar en FV.
Si bé no és molt corrent, s’estima que als EUA hi ha al voltant de deu casos/any d’aquest commotio cordis. És una altra causa de mort sobtada que podem evitar si fer RCP de forma precoç i adequada. Esperem que aquesta entrada serveixi per estar alerta i evitar alguna mort prematura.